Название компании: Eliem Therapeutics
Индустрия: здравоохранение
Год основания: 2018
Количество сотрудников компании: 25
Дата IPO: 06.08.2021, пятница
Доступно через "Финам"! Подробности нижеБиржа: NASDAQ
Тикер: ELYM
Цена размещения: $17-19
Привлекаемая сумма: $72,6 млн ($83,9 млн в случае реализации опционов андеррайтеров) после вычета расходов по размещению и комиссий андеррайтера.
Компания использует полученные средства на финансирование разработки препаратов ETX-810 и ETX-155, доклинические испытания, а также на общие корпоративные целиОбъем размещения: 4 500 000 обыкновенных акций. Компания также предоставила андеррайтерам 30-дневный опцион на покупку дополнительных 675 000 акций
Количество акций после размещения: 23 458 226 обыкновенных акций
Прогнозная рыночная капитализация: $422,2 млн (исходя из средней цены размещения $18)
Андеррайтеры: SVB Leerink LLC, Evercore Group L.L.C., Stifel, Nicolaus & Company, Guggenheim Securities LLC.
Проспект эмиссии
Официальный сайт компании

Eliem Therapeutics - американская биотехнологическая компания клинической стадии, занимающаяся разработкой препаратов для лечения повышенной нервной возбудимости и ассоциируемых с ней расстройств: хронической боли, эпилепсии и других нарушений периферической и центральной нервной системы.
Двумя ведущими препаратами-кандидатами Eliem являются ETX-810 и ETX-155. ETX-810 представляет собой пролекарство (пальмитоилэтаноламид (PEA), первоначально разработанное для лечения диабетической периферической невропатической боли (DPNP) и боли, связанной с пояснично-крестцовой радикулопатией (LSR, также называемой ишиасом). ETX-810 оценивается в двух клинических испытаниях фазы 2a, которые, как ожидается, представят первоначальные данные в первой половине 2022 года. ETX-155 - это аллостерический модулятор (PAM), первоначально разрабатываемый для лечения большого депрессивного расстройства (БДР), перименопаузальной депрессии (ПМД) и фокальных приступов (FOS) - наиболее распространенного проявления эпилепсии. Eliem планирует начать два клинических исследования фазы 2а для ETX-155 в рамках лечения пациентов с БДР и ПМД, которые, как ожидается, представят данные в первой половине 2023 года, и клиническое исследование фазы 1b в рамках лечения пациентов с светочувствительной эпилепсией (окончание в первой половине 2022 года).
Программы исследований Eliem Therapeutics
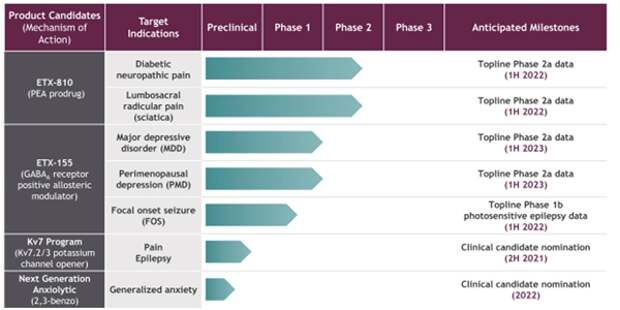
Источник: форма S-1 Eliem Therapeutics
Рынок
Несмотря на объемный глобальный рынок рецептурных препаратов для лечения хронической боли, который, по прогнозам, достигнет примерно $27 млрд в ближайшем десятилетии, менее половины пациентов достигают 50-процентного снижения интенсивности своей боли с помощью текущих терапий первой линии. Помимо неоптимальной эффективности, современные методы лечения часто сдерживаются ограничивающими дозу побочными эффектами, такими как головокружение, седативный эффект, когнитивные нарушения, желудочно-кишечные расстройства и так далее.
Несмотря на эти проблемы, препараты для лечения хронической боли, такие как Lyrica и Cymbalta, достигли значительного коммерческого успеха и вошли в число самых продаваемых фармацевтических продуктов во всем мире: оба препарата достигли годового объема продаж более $5 млрд до потери исключительных прав на патент. Использование пальмитоилэтаноламида (ПЭА), который, как полагают, играет важную роль в регуляции нейровоспаления и передачи сигналов боли, представляет собой многообещающий потенциальный механизм для лечения множественных состояний хронической боли.
ПЭА - это эндогенный биоактивный липид, который был оценен в отношении различных болевых состояний в более чем 30 клинических исследованиях с участием более 2500 пациентов. 15 из этих исследований были рандомизированными контролируемыми исследованиями (РКИ) с участием примерно 1500 пациентов, причем 13 из этих РКИ продемонстрировали статистически значимое улучшение. Несмотря на многообещающие прецедентные клинические данные, на данный момент на глобальных рынках нет терапевтических средств на основе ПЭА, одобренных Управлением по контролю за продуктами и лекарствами США (FDA), Европейским агентством по лекарственным средствам (EMA) или аналогичными регулирующими органами. ПЭА в настоящее время доступен только в виде пищевой добавки. Как пролекарство ПЭА, ETX-810, таким образом, сохраняет значительный потенциал в случае дальнейшего прогресса и успешных результатов клинических испытаний.
Вторая клиническая программа, ETX-155, представляет собой исследуемый пероральный нейроактивный стероид NCE, который действует как положительный аллостерический модулятор рецептора GABAA (GABAAR) и который планируется развивать для лечения пациентов с депрессией и эпилепсией. Депрессивное расстройство поражает примерно 35 млн человек во всем мире и примерно 19 млн человек в США. Несмотря на наличие методов лечения пациентов, страдающих депрессией, имеется значительная вариабельность реакции больных, в результате чего только примерно одна треть пациентов получает пользу от терапии первой линии. Существует острая потребность в безопасных, хорошо переносимых и быстродействующих антидепрессантах, которые надежно обеспечивают клиническое улучшение в срок до шести недель. Эпилепсия же, как второе исследуемое показание ETX-155, поражает примерно 4,7 млн человек в США, Европе и Японии, причем примерно у 1 млн из этих пациентов наблюдается неконтролируемый ФОС, невосприимчивый к противосудорожным препаратам. Несмотря на насыщенный рынок, примерно 30% пациентов с эпилепсией не могут достичь адекватного контроля над приступами.
Как узнать, какие компании и когда выходят на IPO в Америке?
Финансовое положение
Ключевые финансовые показатели компании за последние несколько лет представлены на рисунке ниже.
Основные показатели финансовой отчетности Eliem Therapeutics, тыс. $
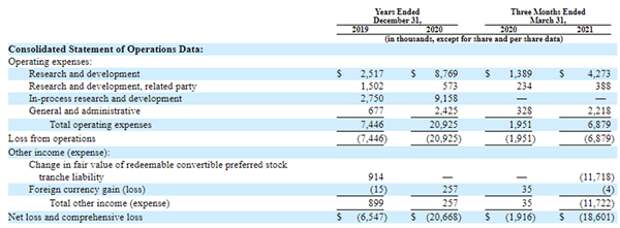
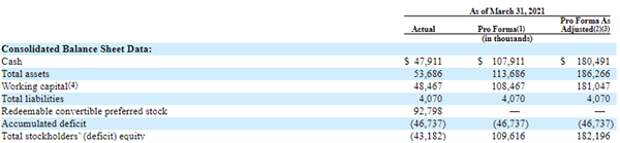
Источник: форма S-1 Eliem Therapeutics
Финансовое состояние Eliem обладает присущими биотехнологическим компаниям ранних стадий характеристиками: выручка не генерируется, а деятельность финансируется за счет выпуска дополнительных конвертируемых привилегированных акций. Накопленный дефицит собственного капитала на конец марта 2021 года составил $46,7 млн: его абсолютное значение, таким образом, составляет 87% от валюты баланса. Среди положительных сторон структуры баланса отметим полное отсутствие долговых обязательств.
Факторы риска
Среди ключевых факторов риска инвестиций в IPO Eliem Therapeutics мы отмечаем следующее:
- Неустойчивое финансовое состояние может вынудить компанию остановить исследовательские программы в случае отсутствия надлежащего внешнего финансирования. Несмотря на то, что последние финансовые отчеты компании были подготовлены, исходя из суждения, что операционная деятельность Eliem будет продолжена, PwC, являющаяся аудитором компании, отметила существенные финансовые риски, обусловленные систематической убыточностью и отрицательными финансовыми потоками. В связи с этим PwC отмечает, что "имеются значительные сомнения по вопросу того, сможет ли Eliem Therapeutics продолжить операционную деятельность".
- Препараты компании находятся на стадиях клинических испытаний и, по собственным оценкам Eliem Therapeutics, с большой вероятностью не будут выведены на рынок раньше 2023 года;
- Рынок болеутоляющих средств является одним из самых конкурентных в отрасли здравоохранения, что создает значительные риски в рамках будущего "принятия" препаратов Eliem Therapeutics потребителями;
- Прочие риски, связанные с регулятивной средой, юридическими и налоговыми обязательствами и т. д.
Принять участие в IPO
Заявки на участие в IPO Eliem Therapeutics принимаются через личный кабинет ФГ "ФИНАМ" до 17:30 мск 5 августа 2021 года.
Минимальная сумма покупки акций составляет $1000, верхний порог не ограничен. Размер брокерской комиссии составляет 5% от суммы сделки.
Инструкция по подаче заявки:
- Авторизуйтесь в личном кабинете.
- Выберите раздел "Услуги".
- Перейдите в подраздел "Операции с ценными бумагами".
- Нажмите на иконку "Участие в IPO".
- Выберите карточку с названием эмитента и нажмите "Участвовать".
- Выберите необходимый счет, укажите сумму заявки и подпишите поручение.
Участие в размещении доступно клиентам со статусом "Квалифицированный инвестор" (ЕДП, обычные счета). Покупка акций с ИИС недоступна.
Подробную информацию об участии в IPO уточняйте у клиентского менеджера. Возможность участия в IPO (англоязычный термин, обозначающий процедуру первичного публичного размещения ценных бумаг) доступна клиентам АО "ФИНАМ" и АО "Банк ФИНАМ" (далее - "Компании"), имеющим статус квалифицированного инвестора. Финансовые инструменты иностранных эмитентов, размещаемые в процессе IPO, могут быть не квалифицированы в качестве ценных бумаг в соответствии с законодательством РФ. Компании не несут ответственность за возможные изменения в процедуре IPO. В условиях ограниченного предложения и непредсказуемого спроса, исполнение заявок на участие в IPO (в том числе, полное или частичное) не может быть гарантировано. Перед принятием решения о приобретении финансовых инструментов посредством участия в IPO, рекомендуем оценить сопутствующие риски, в том числе, внимательно ознакомиться с Декларацией о рисках, связанных с приобретением иностранных ценных бумаг и (или) Декларацией о рисках, связанных с операциями с иностранными финансовыми инструментами, являющимися приложениями к Регламенту брокерского обслуживания.Название компании: Eliem Therapeutics
Индустрия: здравоохранение
Год основания: 2018
Количество сотрудников компании: 25
Дата IPO: 06.08.2021, пятница
Доступно через "Финам"! Подробности нижеБиржа: NASDAQ
Тикер: ELYM
Цена размещения: $17-19
Привлекаемая сумма: $72,6 млн ($83,9 млн в случае реализации опционов андеррайтеров) после вычета расходов по размещению и комиссий андеррайтера. Компания использует полученные средства на финансирование разработки препаратов ETX-810 и ETX-155, доклинические испытания, а также на общие корпоративные цели
Объем размещения: 4 500 000 обыкновенных акций. Компания также предоставила андеррайтерам 30-дневный опцион на покупку дополнительных 675 000 акций
Количество акций после размещения: 23 458 226 обыкновенных акций
Прогнозная рыночная капитализация: $422,2 млн (исходя из средней цены размещения $18)
Андеррайтеры: SVB Leerink LLC, Evercore Group L.L.C., Stifel, Nicolaus & Company, Guggenheim Securities LLC.
Проспект эмиссии
Официальный сайт компании

Eliem Therapeutics - американская биотехнологическая компания клинической стадии, занимающаяся разработкой препаратов для лечения повышенной нервной возбудимости и ассоциируемых с ней расстройств: хронической боли, эпилепсии и других нарушений периферической и центральной нервной системы.
Двумя ведущими препаратами-кандидатами Eliem являются ETX-810 и ETX-155. ETX-810 представляет собой пролекарство (пальмитоилэтаноламид (PEA), первоначально разработанное для лечения диабетической периферической невропатической боли (DPNP) и боли, связанной с пояснично-крестцовой радикулопатией (LSR, также называемой ишиасом). ETX-810 оценивается в двух клинических испытаниях фазы 2a, которые, как ожидается, представят первоначальные данные в первой половине 2022 года. ETX-155 - это аллостерический модулятор (PAM), первоначально разрабатываемый для лечения большого депрессивного расстройства (БДР), перименопаузальной депрессии (ПМД) и фокальных приступов (FOS) - наиболее распространенного проявления эпилепсии. Eliem планирует начать два клинических исследования фазы 2а для ETX-155 в рамках лечения пациентов с БДР и ПМД, которые, как ожидается, представят данные в первой половине 2023 года, и клиническое исследование фазы 1b в рамках лечения пациентов с светочувствительной эпилепсией (окончание в первой половине 2022 года).
Программы исследований Eliem Therapeutics
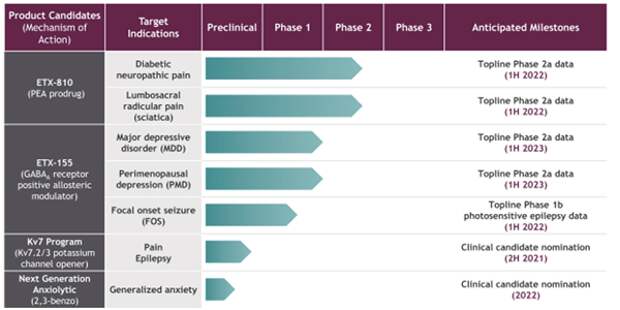
Источник: форма S-1 Eliem Therapeutics
Рынок
Несмотря на объемный глобальный рынок рецептурных препаратов для лечения хронической боли, который, по прогнозам, достигнет примерно $27 млрд в ближайшем десятилетии, менее половины пациентов достигают 50-процентного снижения интенсивности своей боли с помощью текущих терапий первой линии. Помимо неоптимальной эффективности, современные методы лечения часто сдерживаются ограничивающими дозу побочными эффектами, такими как головокружение, седативный эффект, когнитивные нарушения, желудочно-кишечные расстройства и так далее.
Несмотря на эти проблемы, препараты для лечения хронической боли, такие как Lyrica и Cymbalta, достигли значительного коммерческого успеха и вошли в число самых продаваемых фармацевтических продуктов во всем мире: оба препарата достигли годового объема продаж более $5 млрд до потери исключительных прав на патент. Использование пальмитоилэтаноламида (ПЭА), который, как полагают, играет важную роль в регуляции нейровоспаления и передачи сигналов боли, представляет собой многообещающий потенциальный механизм для лечения множественных состояний хронической боли.
ПЭА - это эндогенный биоактивный липид, который был оценен в отношении различных болевых состояний в более чем 30 клинических исследованиях с участием более 2500 пациентов. 15 из этих исследований были рандомизированными контролируемыми исследованиями (РКИ) с участием примерно 1500 пациентов, причем 13 из этих РКИ продемонстрировали статистически значимое улучшение. Несмотря на многообещающие прецедентные клинические данные, на данный момент на глобальных рынках нет терапевтических средств на основе ПЭА, одобренных Управлением по контролю за продуктами и лекарствами США (FDA), Европейским агентством по лекарственным средствам (EMA) или аналогичными регулирующими органами. ПЭА в настоящее время доступен только в виде пищевой добавки. Как пролекарство ПЭА, ETX-810, таким образом, сохраняет значительный потенциал в случае дальнейшего прогресса и успешных результатов клинических испытаний.
Вторая клиническая программа, ETX-155, представляет собой исследуемый пероральный нейроактивный стероид NCE, который действует как положительный аллостерический модулятор рецептора GABAA (GABAAR) и который планируется развивать для лечения пациентов с депрессией и эпилепсией. Депрессивное расстройство поражает примерно 35 млн человек во всем мире и примерно 19 млн человек в США. Несмотря на наличие методов лечения пациентов, страдающих депрессией, имеется значительная вариабельность реакции больных, в результате чего только примерно одна треть пациентов получает пользу от терапии первой линии. Существует острая потребность в безопасных, хорошо переносимых и быстродействующих антидепрессантах, которые надежно обеспечивают клиническое улучшение в срок до шести недель. Эпилепсия же, как второе исследуемое показание ETX-155, поражает примерно 4,7 млн человек в США, Европе и Японии, причем примерно у 1 млн из этих пациентов наблюдается неконтролируемый ФОС, невосприимчивый к противосудорожным препаратам. Несмотря на насыщенный рынок, примерно 30% пациентов с эпилепсией не могут достичь адекватного контроля над приступами.
Как узнать, какие компании и когда выходят на IPO в Америке?
Финансовое положение
Ключевые финансовые показатели компании за последние несколько лет представлены на рисунке ниже.
Основные показатели финансовой отчетности Eliem Therapeutics, тыс. $
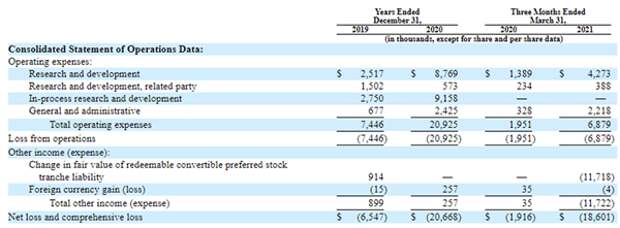
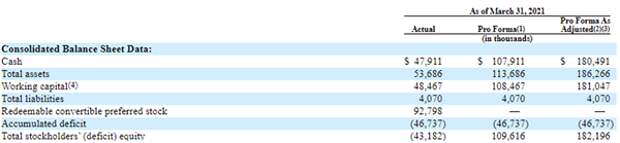
Источник: форма S-1 Eliem Therapeutics
Финансовое состояние Eliem обладает присущими биотехнологическим компаниям ранних стадий характеристиками: выручка не генерируется, а деятельность финансируется за счет выпуска дополнительных конвертируемых привилегированных акций. Накопленный дефицит собственного капитала на конец марта 2021 года составил $46,7 млн: его абсолютное значение, таким образом, составляет 87% от валюты баланса. Среди положительных сторон структуры баланса отметим полное отсутствие долговых обязательств.
Факторы риска
Среди ключевых факторов риска инвестиций в IPO Eliem Therapeutics мы отмечаем следующее:
- Неустойчивое финансовое состояние может вынудить компанию остановить исследовательские программы в случае отсутствия надлежащего внешнего финансирования. Несмотря на то, что последние финансовые отчеты компании были подготовлены, исходя из суждения, что операционная деятельность Eliem будет продолжена, PwC, являющаяся аудитором компании, отметила существенные финансовые риски, обусловленные систематической убыточностью и отрицательными финансовыми потоками. В связи с этим PwC отмечает, что "имеются значительные сомнения по вопросу того, сможет ли Eliem Therapeutics продолжить операционную деятельность".
- Препараты компании находятся на стадиях клинических испытаний и, по собственным оценкам Eliem Therapeutics, с большой вероятностью не будут выведены на рынок раньше 2023 года;
- Рынок болеутоляющих средств является одним из самых конкурентных в отрасли здравоохранения, что создает значительные риски в рамках будущего "принятия" препаратов Eliem Therapeutics потребителями;
- Прочие риски, связанные с регулятивной средой, юридическими и налоговыми обязательствами и т. д.
Принять участие в IPO
Заявки на участие в IPO Eliem Therapeutics принимаются через личный кабинет ФГ "ФИНАМ" до 17:30 мск 5 августа 2021 года.
Минимальная сумма покупки акций составляет $1000, верхний порог не ограничен. Размер брокерской комиссии составляет 5% от суммы сделки.
Инструкция по подаче заявки:
- Авторизуйтесь в личном кабинете.
- Выберите раздел "Услуги".
- Перейдите в подраздел "Операции с ценными бумагами".
- Нажмите на иконку "Участие в IPO".
- Выберите карточку с названием эмитента и нажмите "Участвовать".
- Выберите необходимый счет, укажите сумму заявки и подпишите поручение.
Участие в размещении доступно клиентам со статусом "Квалифицированный инвестор" (ЕДП, обычные счета). Покупка акций с ИИС недоступна.
Подробную информацию об участии в IPO уточняйте у клиентского менеджера. Возможность участия в IPO (англоязычный термин, обозначающий процедуру первичного публичного размещения ценных бумаг) доступна клиентам АО "ФИНАМ" и АО "Банк ФИНАМ" (далее - "Компании"), имеющим статус квалифицированного инвестора. Финансовые инструменты иностранных эмитентов, размещаемые в процессе IPO, могут быть не квалифицированы в качестве ценных бумаг в соответствии с законодательством РФ. Компании не несут ответственность за возможные изменения в процедуре IPO. В условиях ограниченного предложения и непредсказуемого спроса, исполнение заявок на участие в IPO (в том числе, полное или частичное) не может быть гарантировано. Перед принятием решения о приобретении финансовых инструментов посредством участия в IPO, рекомендуем оценить сопутствующие риски, в том числе, внимательно ознакомиться с Декларацией о рисках, связанных с приобретением иностранных ценных бумаг и (или) Декларацией о рисках, связанных с операциями с иностранными финансовыми инструментами, являющимися приложениями к Регламенту брокерского обслуживания.
Свежие комментарии